
題目列表(包括答案和解析)
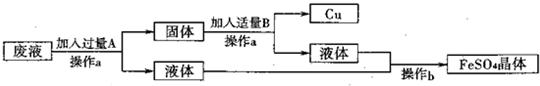



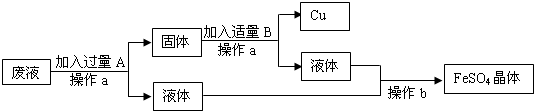
| 操作步驟 | 目的 |
| ①將廢水過濾 | ① 除去不溶性雜質 |
| ②向濾液中加入過量鐵粉 | ② 與硫酸銅完全反應 |
| ③ 過濾 |
③將Cu和過量的鐵粉與FeSO4溶液分離 |
| ④在過濾后固體混合物中加入過得量稀硫酸 | ④ 除去過量的鐵 |
| ⑤將反應后的混合物過濾 | ⑤ 得到硫酸亞鐵溶液和銅 |
| ⑥ 將濾液蒸發結晶 |
⑥得到硫酸亞鐵晶體 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com