
�}Ŀ�б�(�����𰸺ͽ���)
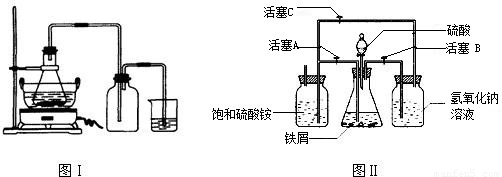
| ��̖ | ������������n��ʾ�������� | �aƷ�|�� |
| 1 | n��H2SO4����n��Fe����1��1 | ����1������֮�g |
| 2 | n��H2SO4����n��Fe����1��1 | ����1�� |
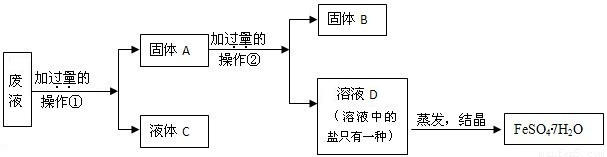

| ��̖ | ������������n��ʾ�������� | �aƷ�|�� |
| 1 | n��H2SO4����n��Fe����1��1 | ����1������֮�g |
| 2 | n��H2SO4����n��Fe����1��1 | ����1�� |

����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com